Кључна разлика: Киселине и базе су две врсте корозивних супстанци. Свака супстанца која има пХ вредност између 0 до 7 сматра се киселом, док је пХ вредност од 7 до 14 база. Киселине су јонска једињења која се раздвајају у води да би се формирао водонични јон (Х +). Јонска једињења су једињења са позитивним или негативним набојем. Базе, с друге стране, су јонска једињења која се раздвајају и формирају негативно набијени хидроксидни ион (ОХ-) у води.

Све хемијске супстанце имају пХ вредност. Скала пХ се креће од 0 до 14. То је мјера концентрације водикових иона у отопини. Свака супстанца изнад неутралног пХ сматра се базом, док се свака супстанца испод неутралног пХ сматра киселином. Неутрални пХ је пХ чисте воде, тј. 7. Свака супстанца која има пХ вредност између 0 до 7 се сматра киселом, док је пХ вредност од 7 до 14 база.
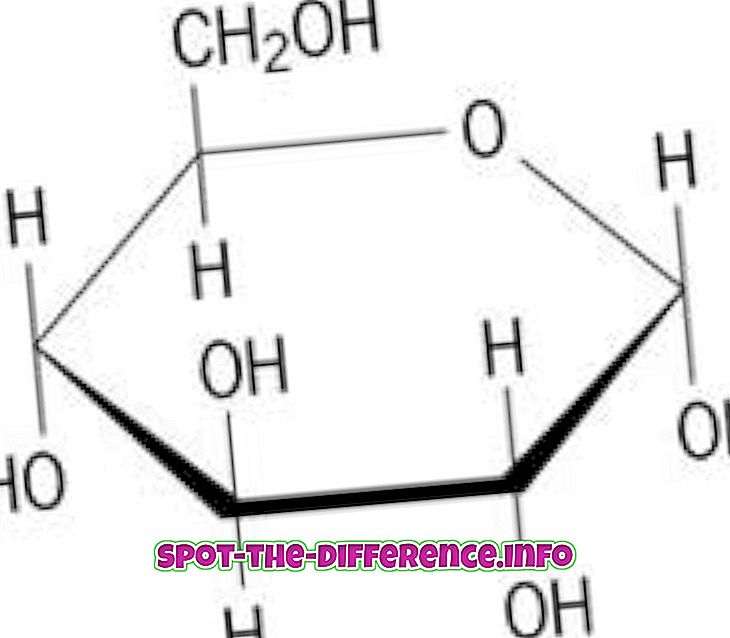
Киселине су јонска једињења која се раздвајају у води да би се формирао водонични јон (Х +). Јонска једињења су једињења са позитивним или негативним набојем. Базе, с друге стране, су јонска једињења која се раздвајају и формирају негативно набијени хидроксидни ион (ОХ-) у води. Јачина киселине или базе се одређује на основу тога колико ослобађају њихове одговарајуће јоне; што је више јона, то су јачи.
Осим тога, ако се комбинују киселине и базе исте јакости, оне имају тенденцију да производе со и воду. На пример: ХЦл (киселина) + НаОх (база) = НаЦл (сол за домаћинство) + Х2О (вода)
Карактеристике киселина:
- окусити кисело када се једу
- могу да убоде кожу када се додирну
- може кородирати (или појести) метале и кожу
- може се користити као реактант током електролизе због присуства покретних иона
- окрените плави лакмус папир црвено
- студирају у хемији и биологији
- на универзалном индикатору постаје црвена или наранџаста
Киселине се могу сврстати у:
- Јаке киселине - најчешће су сумпорна киселина, азотна киселина и хлороводонична киселина (Х2СО4, ХНО3, односно ХЦл).
- Неке концентроване слабе киселине, на пример мравља киселина и сирћетна киселина
- Снажне Левис киселине као што је анхидровани алуминијум хлорид и бор трифлуорид
- Левис киселине са специфичном реактивношћу, нпр. Раствори цинковог хлорида
- Изузетно јаке киселине (суперкиселине)

- Горак укус (за разлику од киселог укуса киселина)
- Слузав или сапунски прст на прстима
- Многе базе реагују са киселинама и преципитирају соли.
- Јаке базе могу бурно реаговати са киселинама. Просути киселину може се безбедно неутралисати коришћењем благе базе.
- Базе претварају црвени лакмус папир у плаво
- Базе су супстанце које садрже металне оксиде или хидроксиде
- Базе које су растворљиве у води формирају алкалије (растворљиве базе)
Базе се могу сврстати у:
- Каустика или алкалије, као што су натријум хидроксид (НаОХ) и калијум хидроксид (КОХ)
- Алкални метали у металној форми (нпр. Елементарни натријум) и хидриди алкалних и земноалкалних метала, као што је натријум хидрид, функционишу као јаке базе и хидрирају да дају каустику
- Изузетно јаке базе (супер-суперзе) као што су алкоксиди, метални амиди (нпр. Натријум амид) и органометалне базе као што је бутилитијум
- Неке концентроване слабе базе, као што је амонијак када су безводне или у концентрованом раствору
Ацид | Басе | |
Аррхениус Дефинитион | Киселина је било које хемијско једињење које, када се раствори у води, даје раствор са активношћу јона водоника већом него у чистој води. | База је водена супстанца која може да прихвати јоне водоника. |
Бронстеад Ловри Дефинитион | Киселина је супстанца која дарује протон. | База је свака супстанца која прихвата протон. |
пХ вредност | Мање од 7.0 | Више од 7.0 |
Лакмус папир | Плави лакмус папир постаје црвен | црвени лакмус папир постаје плав |
Пхенолпхтхалеин | Остаје безбојан | Раствара раствор |
Дисоцијација (у води) | Киселе слободни јони водоника (Х +) када су помешани са водом. | Базе слободних хидроксидних јона (ОХ-) када су помешане са водом. |
Хемијска формула | Киселина има хемијску формулу са Х на почетку. На пример, ХЦл (Хлороводонична киселина). Постоји један изузетак од његовог правила, ЦХ3ЦООХ = сирћетна киселина (сирће). | База има хемијску формулу са ОХ на крају. На пример, НаОХ (натријум хидроксид). |