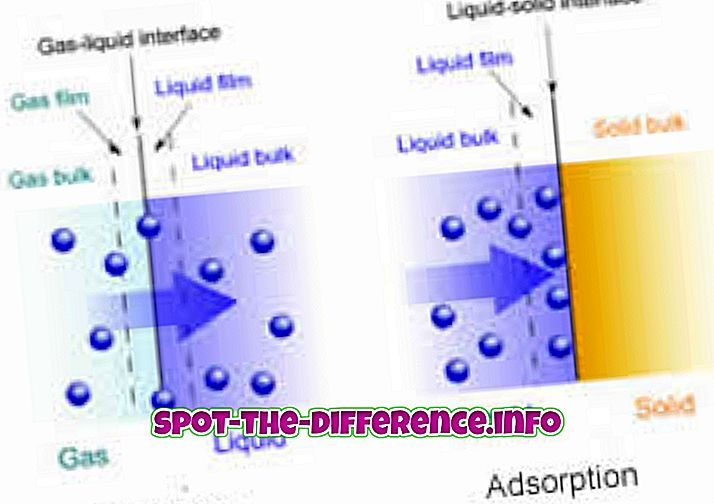
Кључна разлика: Апсорпција је масовни феномен у коме апсорбат потпуно продире у тело чврсте или течне материје да би формирао једињење или раствор. С друге стране, адсорпција је површинска појава у којој се молекули адсорбата концентрирају само на површини адсорбента.
Хемијска реакција - угљен диоксид апсорбује раствор калијумовог угљеника
Физички процес - Ваздух апсорбује у води растварањем

Постоје два типа адсорпционих модова - хемијски и физички. У хемијској адсорпцији, молекули и површина везани су слабим Вандер Валлс силама. С друге стране, у хемијској адсорпцији настаје хемијска веза између молекула и површине.
Дакле, примарна разлика између адсорпције и апсорпције је да је апсорпција расути феномен, што значи да се дешава у цијелом тијелу материјала, док адсорпција остаје површински феномен. Адсорпција је увек егзотермна, док је апсорпција ендотермна. Сорпција укључује оба процеса апсорпције и адсорпције.
Поређење адсорпције и апсорпције:
Адсорпција | Апсорпција | |
Дефиниција | Акумулација гаса или течне раствора на површини чврстог материјала или течности | Дифузија супстанце у течност или чврсту супстанцу да се формира раствор или једињење |
Пример | Инертни гасови се адсорбују на угаљ. | Сува спужва упија воду |
Размена топлоте | Егзотермно са изузетком адсорпције Х2 на стаклу | Ендотхермиц |
Аттаининг Екуилибриум | Компаративно брже | Компаративно полако |
Концентрација | Концентрација на површини адсорбента је различита од оне у маси | Концентрација остаје иста кроз материјал |
Стопа појаве | У почетку је брз, али касније почиње да опада | Она се одвија уједначеној стопи |