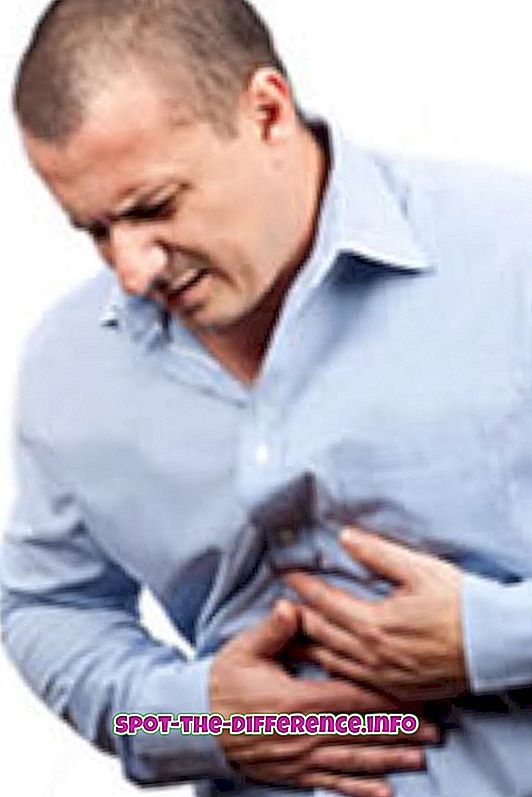
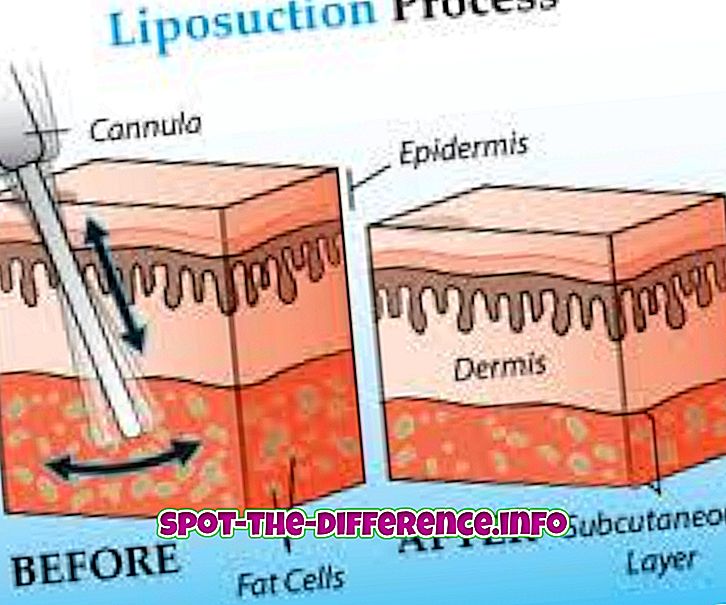
Кључна разлика: Атоми су основне јединице од којих је сва материја направљена. Атоми су малени, у распону од 0.1 до 0.5 нанометара у ширини. Сваки атом било којег елемента је састављен од протона, неутрона и електрона. Атоми различитих елемената се спајају да би направили молекуле. То се дешава путем хемијске реакције. Молекул је најмања количина хемијске супстанце која може постојати.
Елемент је чиста хемијска супстанца која има један или један тип атома, који се разликује по свом атомском броју. Атомски број је изведен из броја протона присутних у језгру елемента. Укупно је идентификовано 118 елемената, подељених између метала, металоида и неметала. Сваки елемент има свој властити скуп својстава. Већина елемената је доступна на Земљи, док је неколико њих развијено умјетно путем нуклеарних реакција. Елемент је већ у најситнијем облику и не може се даље поделити. Сви елементи се могу наћи у Периодном систему, наведеном по атомском броју.
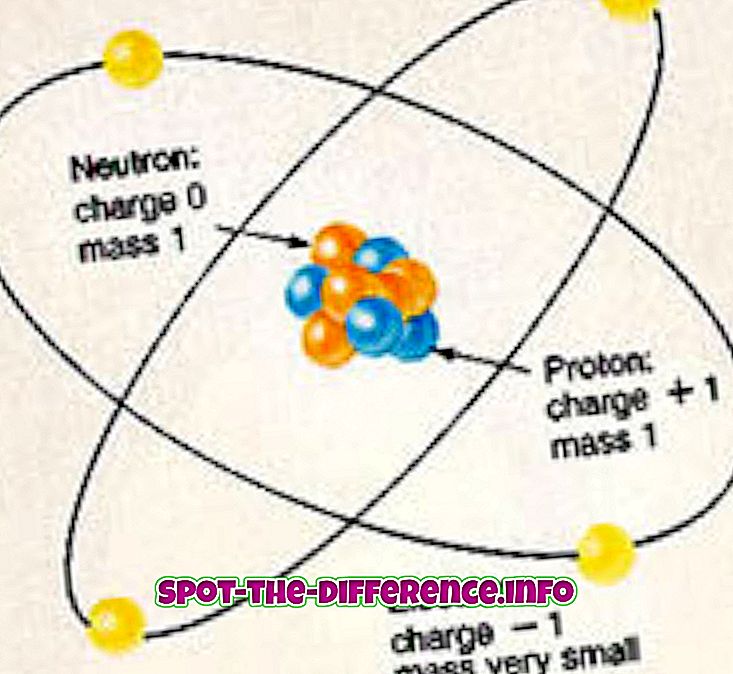
Сваки атом било којег елемента је састављен од протона, неутрона и електрона. Протони и неутрони чине језгро атома и налазе се у средини атома. Језгро је окружено облаком електрона који су електромагнетском силом везани за нуклеус. Електрони имају негативан набој који је привучен нуклеусом, јер протони у језгру имају позитиван набој. Неутрони, с друге стране, немају пуњење.
Број протона, неутрона и електрона у атому одређује који је то елемент. На пример: Атом гвожђа има 26 протона, 30 неутрона и 26 електрона. Сваки атом гвожђа ће имати ову конфигурацију.
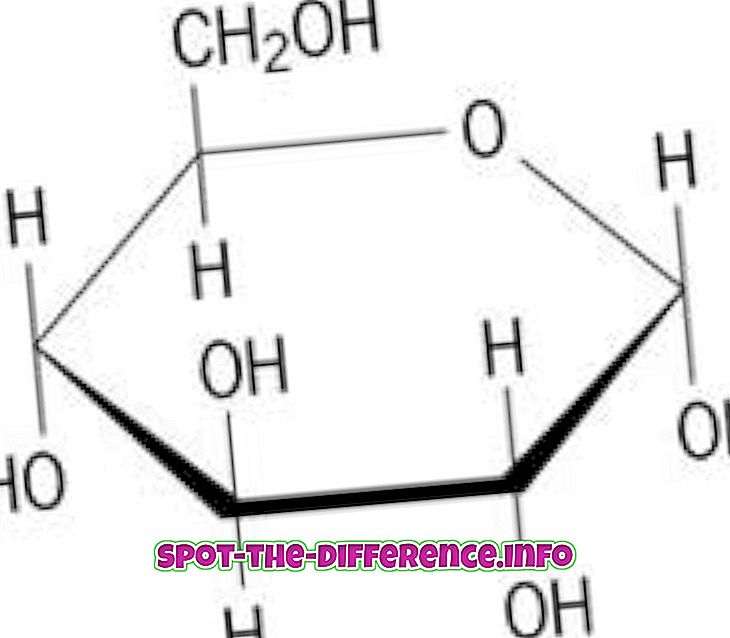
Атоми различитих елемената се спајају да би направили молекуле. То се дешава путем хемијске реакције. На пример: два атома водоника и један атом кисеоника комбинују се да би направили молекул воде.

Молекул може имати веома различита својства од елемената од којих је направљен. На примјер: вода се понаша врло различито од било кисеоника или водика, иако је састављена од два атома водика и једног атома кисеоника.
Штавише, атом не може постојати независно у природи без везивања за нешто. Никада нећемо наћи само један атом кисеоника или један атом угљеника. Увек је везан за нешто, као што је О2 (кисеоник) или ЦО2 (угљен диоксид). Када је везан у молекул, молекул може да постоји независно у природи, због чега увек можемо пронаћи молекул кисеоника, молекула угљен диоксида, молекула воде (Х2О) итд.
У молекулу, атоми су спојени у одређеном облику или форми. То углавном зависи од броја веза које атом може да направи. Атоми формирају молекуле формирањем хемијских веза једна са другом. Атоми кисеоника увек имају две везе са другим атомима, угљеников атом увек има четири везе са другим атомима, а атоми азота увек имају три везе са другим атомима. Због тога одређени тип молекула увек има посебан облик, као што је петерокутна, шестерокутна, латерална, би-латерална, итд.
Молекули увек теже да се групишу, њихова формација зависи од њиховог стања. Као у гасовитом стању, молекули имају тенденцију да само лете около. У течном стању, молекули имају тенденцију да буду лабаво груписани заједно, тако да се и даље могу кретати. Док су у чврстом стању, молекули су чврсто спојени и могу само вибрирати.
Молекули су обично представљени у молекулској формули. На пример: О2, Х2О, ЦО2, Ц6Х12О6 (шећер). Молекуларна формула је име елемента, а затим број атома тог елемента у молекулу.