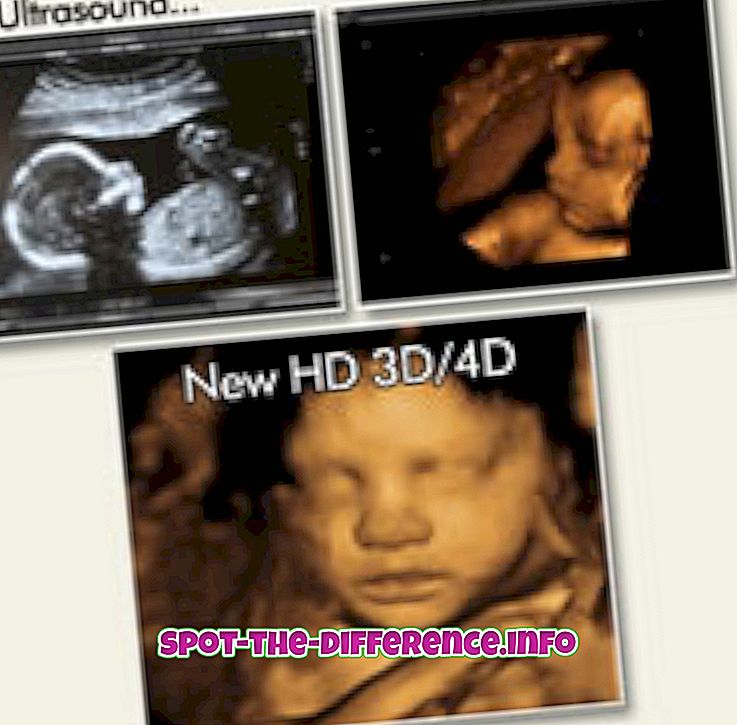
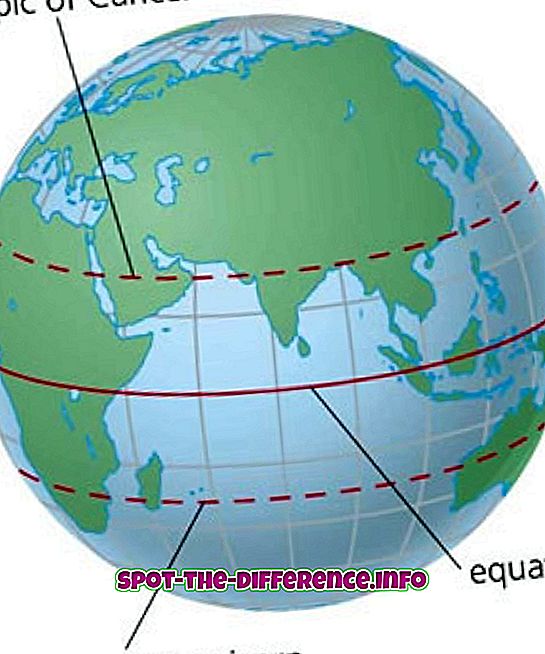
Кључна разлика: Атомска маса је једноставно маса одређеног изотопа, или комбинована маса протона, неутрона и електрона атома. Атомски број је број протона који се налази у језгру елемента.
Признајмо да је хемија збуњујућа, различита количина елемената, атомски бројеви, везе, маса, тежина, атоми, итд. Све ове речи почињу да се замагљују након одређеног времена да особа више не може да разликује једну од друге. Па атомска маса и атомски број су две такве речи које се често збуњују и користе наизменично.
Атомска маса је маса атома када је у мировању. То је зато што када се атом креће веома великом брзином, има тенденцију повећања масе. Иако је према дефиницији атомска маса маса свих протона, неутрона и електрона, електрони су сувише мали да би направили било какву значајну разлику у атомској маси. Већина елемената периодне табеле има изотопе и због разлике у броју неутрона маса сваког изотопа се такође мења.
Атомска маса се изражава помоћу јединица атомске масе или аму. Једна атомска маса је једнака 1/12 масе Царбон-12. Када се маса атома подели са 1/12 маса угљеника-12, добија се релативна маса елемента. Међутим, релативна маса објекта је у ствари атомска тежина елемента, јер се израчунава из свих изотопа. Међутим, то се не би требало сматрати атомском масом елемента.

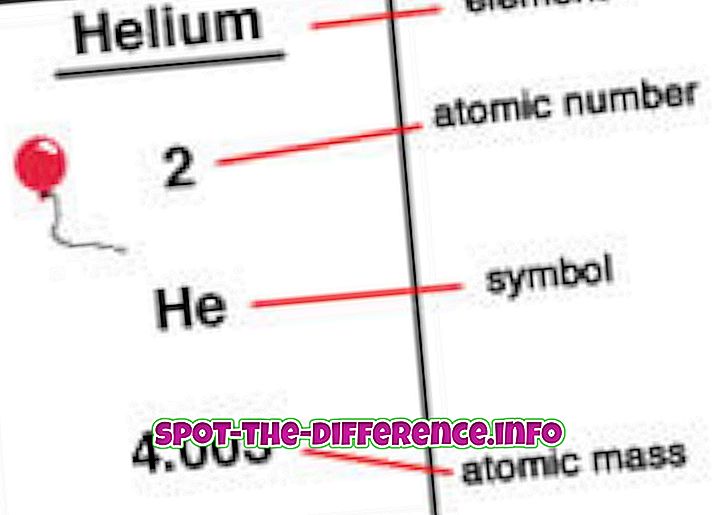
Атомски број је број протона који се налази у језгру елемента. Када је атом неутралан, то значи да има исти број протона и електрона. Атомски број је означен са З. Будући да сваки елемент има различит број протона, овај број се такође користи за представљање елемента. Изотопи обично имају исти атомски број, али су класификовани коришћењем њихове атомске масе, на пример Царбон-12, Царбон-13.
Елементи се постављају у редоследу атомског броја на периодној табели. Атомски број је наведен у горњем левом углу елемента као суперсцрипт. Атомски бројеви могу помоћи у откривању информација о елементу и многи људи могу видјети атомски број и навести који је елемент. Такође се каже где се у периодном систему може поставити и да ли је течна, гасна или чврста. Атомски број такође даје информације о нуклеарном набоју, оксидационим стањима, понашању везивања, набоју јона итд.