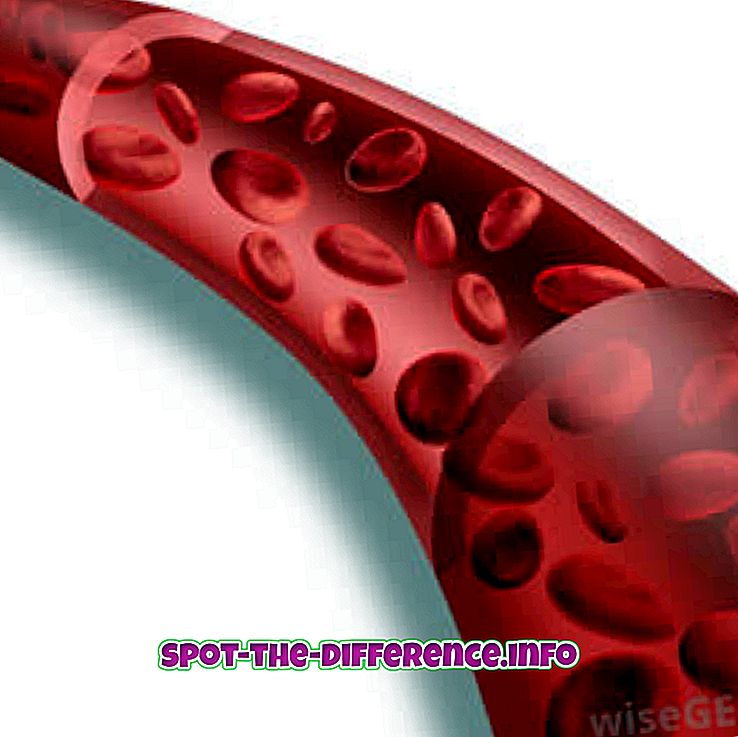
Кључна разлика: 'Спектар за емитовање линије' се добија када се емисија догоди од атома, гдје су линије обично јединствене и различите у природи, док је 'спектар емисије' у облику континуираних трака које се добијају из молекула.

Емисија је процес којим се квантно-механичко стање неке честице више енергије претвара у нижи облик кроз емисију фотона, што доводи до производње светлости. У емисији, спектри светлих линија, трака или континуираних зрачења су карактеристике које се одређују специфичним емитованим супстанцама и подвргавају се одређеној врсти побуде. Ови спектри се добијају из гасова као што су водоник, хелијум, литијум, жива, итд.
Једноставно речено, линијски емисиони спектар састоји се од низа фреквенција електромагнетних зрачења, углавном емитованих од стране елемената, атома или молекула једињења у нижим енергетским стањима. Сваки емисиони спектар у линијској емисији је јединствен и различит у природи.

Спектралне емисијске линије су изузетно корисне у астрономији, физици, квантној механици, хемији, итд. Ове емисије се јасно односе на концепт 'спектроскопске емисије'. Наведена емисија је спектроскопска техника која испитује таласне дужине фотона емитованих од стране атома / молекула током њиховог преласка из узбуђеног стања у стање ниже енергије.
Поређење спектра емисије у линији и спектра емисије у опсегу:
Спектар емисије линија | Спектар емисионог опсега | |
Кратак опис | Спектар за емитовање линија је једноставно различитост фреквенција електромагнетног зрачења које обично емитују атоми елемента или молекули једињења када су у стању ниже енергије. | Спектар спектра зрачења се обично добија из различитих спектара линија који су уско распоређени заједно и који су у континуираном стању. |
Добијен из | Они се добијају преко атома или елемента. | Они се добијају из различитих спектарских линија. |