Кључна разлика: Распоред атома у молекулу помаже у одређивању поларитета. За молекул се каже да је поларни, ако има позитиван и негативан набој. Неполарни молекул је молекул са мање пуњења.
У хемији, поларитет се односи на раздвајање између електричних набоја молекула или његове хемијске групе који имају електрични дипол или вишеполни момент. Поларни молекули интерагују кроз интермолекуларне везе и водикове везе. Молекуларна поларност зависи од разлике у електронегативности између атома у молекулу. Поларитет такође одређује бројне физичке особине као што су површинска напетост, тачке топљења и тачке кључања, и растворљивост.
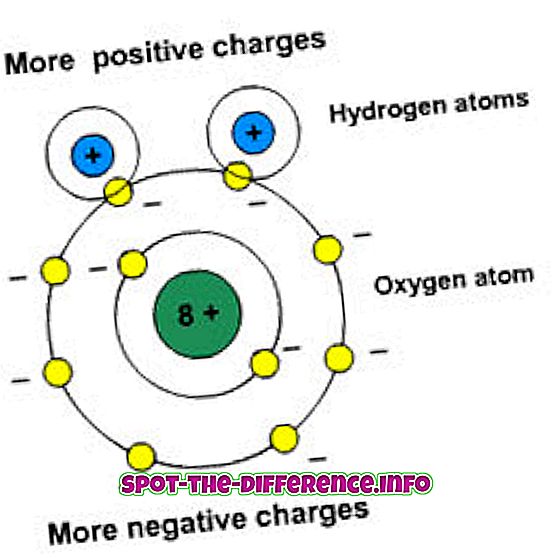
Поларитет значи раздвајање набоја. Ови молекули имају диполни моменат. Диполни моменат мери поларитет везе. Поларне супстанце ступају у интеракцију са другим поларним елементима.

Неполарни молекул нема довољно набоја. Неполарни молекули се распоређују на начин симетрије и немају велики број електричних набоја на њима. Када два атома или два иста атома имају исту електронску везу између њих, атоми повлаче електронски пар. Ова повлачења им помажу да деле електроне и ова врста дељења веза између молекула је позната као неполарна ковалентна веза.
Поређење између поларног и не-поларног:
Полар | Нон-Полар | |
Дефиниција | Поларне супстанце имају позитиван и негативан набој на атому. | Неполарне супстанце немају велике набоје на атому. |
Покрет | Имају електрично диполно кретање. | Они немају никакав диполни покрет. |
Цхарге сепаратион | Постоји раздвајање наплате. | Нема раздвајања наплате. |
Интеракција | Они су у интеракцији са другим поларним супстанцама. | Они нису у интеракцији са другим поларним супстанцама. |
Пример | Вода, алкохол и сумпор. | Оил. |