Кључна разлика: Ионска веза је хемијска веза између два различита (тј. Металног и неметалног) атома у којима један атом предаје електрон другом. Ковалентна веза је друга јака хемијска веза. Догађају се слични атоми (тј. Два неметала). У ковалентној вези два атома се удружују да деле електрон, уместо атома који узима електрон од другог.
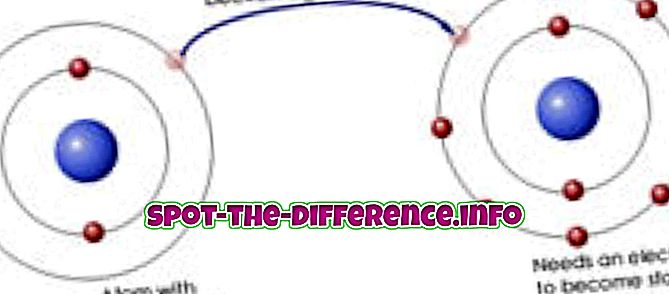
Ионска веза је хемијска веза између два различита (тј. Металног и неметалног) атома у којима један атом предаје електрон другом. Стога оба атома постају јони јер један атом има један електрон мање, док други има екстра. Метални јон који је изгубио електрон има позитиван набој. Не-метални јон који је добио електрон има негативан набој. Како се супротности привлаче, ови иони се онда снажно привлаче једни другима, тако снажно да постану повезани.
Ионска једињења су обично у облику чврстих материја, тј. Соли. Они су високо растворљиви у води и имају високу тачку топљења. Када су у води, имају и високу електричну проводљивост.

Ковалентно везивање обухвата многе врсте интеракција, укључујући σ-везивање, π-везивање, везивање метала на метал, агостичке интеракције и тродимензионалне везе са два електрона. Када атом има свој електрон у својој спољашњој љусци, а други атоми захтевају од електрона да напуни своју спољну љуску, два атома нека заједно деле електрон. Дакле, оба атома имају крајњу спољашњу љуску, а тиме и стабилну електронску конфигурацију.
Хемијске везе су направљене тако да атом може имати пуну спољашњу љуску, јер пуна спољашња љуска значи стабилну електронску конфигурацију. У јонској вези, када метални атом има један електрон у својој спољашњој љусци и неметал треба електрон да испуни своју спољашњу љуску, атом метала даје свој електрон неметалу. Слично томе, у ковалентној вези, они деле електрон једнако.
Јонска веза | Ковалентна веза | |
Дефиниција | Хемијска веза између два различита атома у којима атом предаје електрон другом. | Ковалентна веза је хемијска веза која укључује дељење електрона између два слична атома. |
Оццурренце | Метални и неметални | Два неметала |
Поларитет | Високо | Лов |
Облик молекула | Нема дефинитивног облика, решеткасте структуре | Дефините схапе |
Електрична проводљивост | Високо | Обично нема |
Топлотна проводљивост | Високо | Обично ниско |
Тачка топљења супстанце | Мијења се, али обично је већа од ковалентних спојева | Варира, али обично је нижа од јонских једињења |
Тачка кључања супстанце | Високо | Варира, али обично је нижа од јонских једињења |
Растворљивост у води | Високо | Варира, али обично је нижа од јонских једињења |
Стање супстанце на собној температури | Обично чврсто | Чврста, течна, гас |