Кључна разлика: Моларност, такође позната као моларна концентрација, мери број молова супстанце присутне у литру раствора. Моларност је означена главним М. Молалити мери број молова супстанце присутне у килограму растварача. Молалност се означава малим словом м.
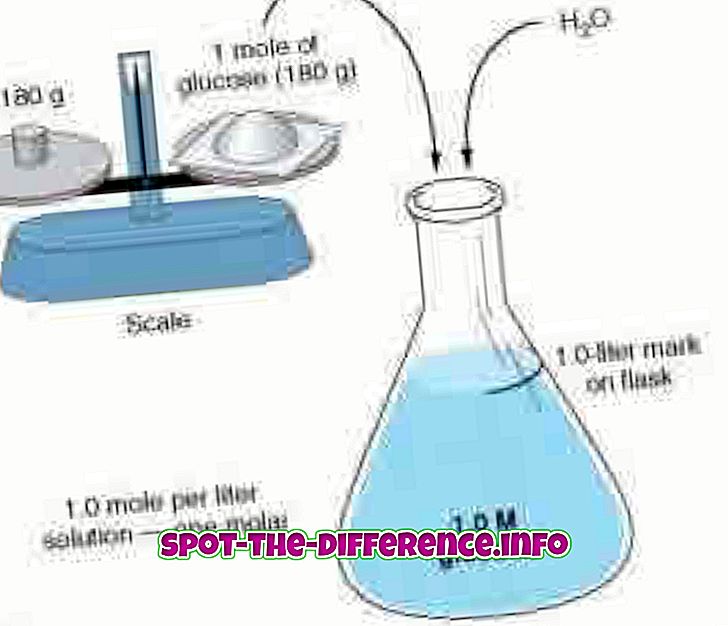
Оба концепта заснивају своје калкулације на томе колико је молова присутно у тренутном решењу. Раствор се може дефинисати као хомогена смеша, што значи да су две или више компоненти мешане до те мере да се не може разликовати голим оком. Ова два концепта захтевају разумевање мола јер одређује број молова присутних у раствору. Теорију кртица открио је италијански научник Амедео Авогардо.
Године 1811. Авогардо је предложио да запремина гаса, при датој температури и притиску, буде пропорционална броју атома или молекула без обзира на његову природу. Овај концепт је познат као Авогардо константа. Дефинише се као број саставних честица (обично атома или молекула) у једном молу дате супстанце. У лаичким терминима, један мол супстанце би представљао број атома и молекула присутних у елементу. На пример: Кисеоник има атомску тежину од 16, што представља масу по молу кисеоника. Тако би један мол кисеоника имао масу од 16 грама. Према Авогарду, један мол кисеоника би имао исти број атома као један мол водоника. Међутим, они се могу разликовати по тежини.
Моларност и молалност мјере концентрацију користећи два различита приступа. Моларност, такође позната као моларна концентрација, мери број молова супстанце присутне у литру раствора. Моларитет се означава са главним М. Дакле, решење са 1.0М наводи да садржи 1 мол раствора по литру раствора. На пример: раствор воде и шећера. Ако се раствор мери 1, 0 М, онда раствор садржи 1 мол шећера по литру присутног раствора. Моларност је такође позната као концентрација количине супстанце, концентрација количине, концентрација супстанце или једноставно концентрација. Моларност се може израчунати помоћу формуле: М = мол (# молова) / Л (запремина раствора у литрима).

Молалност мери број молова супстанце присутне у килограму растварача. Молалност се означава малим словом м. Решење са 1.0м би значило да садржи 1 мол раствора по килограму растварача. Хајде да разликујемо раствор од растварача. Солуте је супстанца која се раствара у другу супстанцу. Растварач је супстанца која раствара раствор. Дакле, ако се вода и шећер меша заједно, шећер би био раствор и вода растварач. Решење би била мешана шећерна вода. Сада, у молалности, од највеће је важности да моли буду подељени на масу растварача, а не на раствор. Молалност се може израчунати користећи формулу: м = мол (# од мола) / КГ (маса растварача у кг).
Зашто је разлика? Па, оба се користе када се ради о температури. Ако се раствор промени у температури онда се користи молалност. Али за отопине које ће остати на константној температури користи се моларност. То је због тога што се температура повећава или пада, волумен отопине се мијења и то директно утјече на моларност. Према томе, молалност се користи за израчунавање концентрације.